- Confirmation du bon profil de sécurité et de tolérance de GS010
- Maintien du gain d’acuité visuelle chez les patients diagnostiqués depuis moins de 2 ans
Paris, 20 décembre 2016 – GenSight Biologics (Euronext : SIGHT, ISIN : FR0013183985, éligible PEA- PME), société biopharmaceutique dédiée à la découverte et au développement de thérapies géniques innovantes pour le traitement des maladies neurodégénératives de la rétine et du système nerveux central, annonce aujourd’hui des résultats complémentaires prometteurs après 78 semaines de suivi de son étude de phase I/II. Ces résultats confirment le bon profil de sécurité et de tolérance de GS010, et démontrent le maintien du gain d’acuité visuelle chez les patients atteints de neuropathie optique héréditaire de Leber (NOHL).
Chaque groupe de trois patients a reçu une dose croissante de GS010 par injection intra vitréenne unique dans l’œil le plus sévèrement atteint par la pathologie. Le recrutement s’est achevé en avril 2015 et le suivi à long terme est en cours. Avant injection, les yeux traités et non-traités présentaient tous une acuité visuelle médiane dite « off-chart »1.
78 semaines après l’injection, on observe un gain moyen d’acuité visuelle par rapport à la baseline de – 0,61 LogMAR (p<0,001) dans l’œil traité de l’ensemble des patients, équivalent à un gain de +30 lettres ETDRS. Dans l’œil non-traité après 78 semaines de suivi, le gain observé est de -0,31 LogMAR (p=0,0866), équivalent à un gain de +15 lettres ETDRS. Il en résulte un effet traitement (différence moyenne entre l’œil traité le plus affecté et l’œil non-traité le moins affecté) de +15 lettres (p=0,11) en faveur de l’œil traité le plus affecté.
|
Variation moyenne de l’acuité visuelle en équivalent Lettre ETDRS (LogMAR) de la baseline à 78 semaines |
OEil traité (TE)Variation moyenne (LogMAR) |
OEil non-traité (TE)Variation moyenne (LogMAR) |
Résultats d’acuité visuelle TE vs UTE |
| Tous patients (n=14) | +30 lettres (-0.61) |
+15 lettres (-0.31) |
+15 lettres (-0.30 LogMAR) |
|
Patients atteints depuis ≤ 2 ans (n=5)* |
+32 lettres (-0.63) |
+12 lettres (-0.23) |
+20 lettres (-0.40 LogMAR) |
Note (*) : Exclut les patients « hand motion »), conformément au protocole de Phase III.
Source : Société
Il est intéressant de noter que, chez les patients atteints depuis moins de 2 ans au moment de l’injection, le gain moyen observé dans l’œil traité est de +32 lettres ETDRS (-0,63 LogMAR), comparé à un gain moyen de +12 lettres ETDRS (-0,23 LogMAR) observé dans l’œil non-traité, soit une différence de 20 lettres ETDRS en faveur de l’œil traité.
Le groupe de patients atteints d’une perte de vision depuis 2 ans ou moins au moment de l’injection présente un effet traitement en faveur de l’œil traité d’amplitude croissante à partir de la semaine 36.
Evolution de l’acuité visuelle de l’œil traité vs œil non-traité après 78 semaines de suivi chez les patients atteints depuis moins de 2 ans
(en nombre équivalent de lettres lues; n=5*)
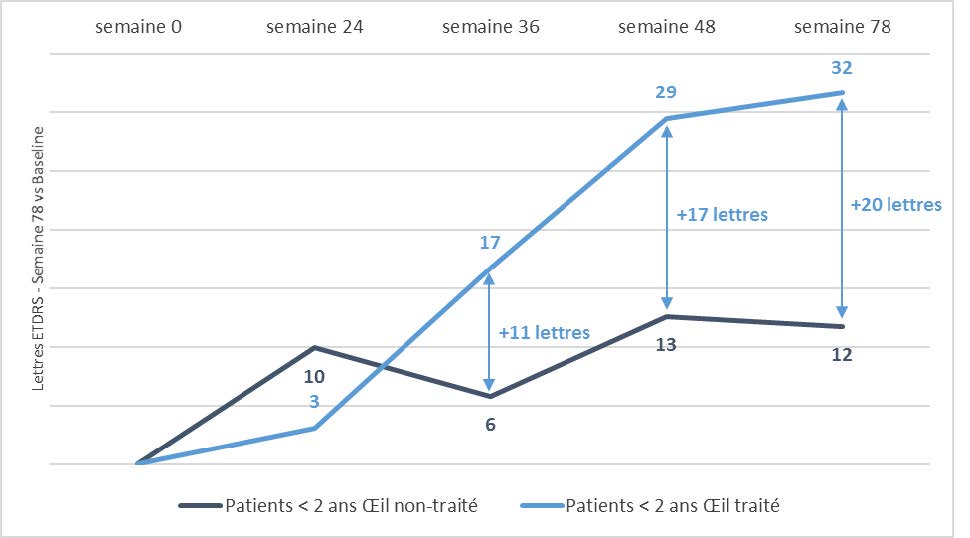
Note (*) : Exclut les patients « hand motion »), conformément au protocole de Phase III.
Source : Société
Bernard Gilly, Directeur Général et cofondateur de GenSight Biologics, commente : « Ces derniers résultats sont très encourageants, et ils confirment un bénéfice clinique durable pour les patients dans ce suivi à long terme. Ces données renforcent encore la pertinence du design de nos deux études de phase III avec GS010 dans le traitement de la neuropathie héréditaire de Leber, en cours aux Etats-Unis et en Europe, avec une prise en charge précoce des patients dans leur perte de vision. Nous sommes très reconnaissants envers les patients et leurs familles pour leur implication dans nos études cliniques. C’est grâce à eux que nous parvenons à développer un traitement pour cette terrible maladie invalidante. »
Dr. Catherine Vignal, investigateur de l’étude et Chef de service d’ophtalmologie à la Fondation Ophtalmologique A. de Rothschild, a ajouté : « Les tendances observées à 48 semaines se confirment après un an et demi de suivi, et renforcent l’espoir des patients atteints de NOHL. Les enseignements tirés de ces résultats, et de ceux à venir, seront déterminants dans le développement par GenSight d’une thérapie pour cette maladie très sévère pour laquelle aucun traitement curatif n’existe à ce jour.”
GenSight Biologics conduit actuellement deux études cliniques de phase III (Rescue et Reverse) en Europe et aux États-Unis pour évaluer l’efficacité de GS010 chez des sujets atteints de la NOHL induite par la mutation ND4, et ayant subi une perte d’acuité visuelle depuis moins d’un an. La fin du recrutement est prévue pour Q1 2017 pour les deux études.
À propos de GenSight Biologics
GenSight Biologics S.A. (GenSight Biologics) est une société biopharmaceutique dédiée à la découverte et au développement de thérapies géniques innovantes pour le traitement des maladies neurodégénératives de la rétine et du système nerveux central. Le portefeuille de recherche de GenSight Biologics s’appuie sur deux plates-formes technologiques : le ciblage mitochondrial (Mitochondrial Targeting Sequence, ou MTS) et l’optogénétique, visant à préserver ou restaurer la vision chez les patients atteints de maladies neurodégénératives de la rétine. Le candidat médicament le plus avancé de GenSight Biologics, GS010, est en Phase III pour le traitement de la neuropathie optique héréditaire de Leber (NOHL), une maladie mitochondriale rare qui conduit à une perte irréversible de la vue chez les adolescents et les jeunes adultes. En utilisant son approche de thérapie génique, les candidats médicaments de GenSight Biologics sont destinés à offrir aux patients une récupération visuelle fonctionnelle durable après une seule injection intravitréenne dans chaque œil.
À propos de GS010
GS010 cible la neuropathie optique héréditaire de Leber (NOHL), une maladie mitochondriale rare, de transmission maternelle, caractérisée par une dégénérescence des cellules ganglionnaires de la rétine et provoquant en moins d’un an une perte brutale et irréversible de la vision conduisant généralement à la cécité légale. Ces symptômes apparaissent principalement chez les adolescents et les jeunes adultes. GS010 s’appuie sur une technologie propriétaire de séquence de ciblage mitochondrial (MTS), issue des travaux de l’Institut de la Vision, qui, lorsqu’elle est associée au gène d’intérêt, permet de l’adresser spécifiquement à l’intérieur de la mitochondrie grâce à un vecteur AAV (Adeno-Associated Virus). Le gène d’intérêt est ainsi transféré dans la cellule pour y être exprimé et produire la protéine fonctionnelle, qui sera acheminée à l’intérieur des mitochondries grâce aux séquences nucléotidiques spécifiques, afin de restaurer la fonction mitochondriale déficiente ou manquante.
–
1 Avant injection (baseline), l’œil traité le plus affecté présentait une acuité visuelle médiane de 2,79 LogMAR (approximativement équivalent à un mouvement de la main à 1m) et l’œil non-traité le moins affecté présentait une acuité visuelle médiane de 2,01 LogMAR (approximativement équivalent à compter des doigts à 50cm).
Contacts
-
GenSight BiologicsDirecteur Administratif et FinancierThomas Gidoin+33 (0)1 76 21 72 20