Paris, France, le mercredi 20 Juillet 2022, 7h30 CEST – GenSight Biologics (Euronext : SIGHT, ISIN : FR0013183985, éligible PEA-PME), société biopharmaceutique dédiée au développement et à la commercialisation de thérapies géniques innovantes pour les maladies neurodégénératives de la rétine et du système nerveux central, annonce aujourd’hui que des sujets atteints de Neuropathie Optique Héréditaire de Leber (NOHL) traités avec LUMEVOQ® continuent à bénéficier d’une nette amélioration de leur vision 5 ans après une seule injection de la thérapie génique. Comparés à l’évolution de la vision observée chez les patients non traités1, ces résultats diffèrent de façon importante par rapport à l’histoire naturelle de la NOHL.
Les données de RESTORE (CLIN06) 2, l’étude de suivi à long terme à laquelle tous les participants aux études pivotales de Phase III RESCUE3 et REVERSE4 ont été invités, continuent également de montrer que le traitement est bien toléré sur la période de suivi de 5 ans.
Les données sur l’efficacité et l’innocuité recueillies sur 5 ans constituent des preuves substantielles de durabilité et sont plus complètes que ce qui est généralement soumis dans un dossier de données pour une thérapie génique.
Lorsque les sujets ont intégré l’étude RESTORE, 2 ans après l’injection unique, ils présentaient déjà des améliorations cliniquement significatives par rapport au point le plus bas (le « nadir* ») de leur acuité visuelle (BCVA) : +18,8 lettres ETDRS** dans les yeux traités par LUMEVOQ® et +17,3 lettres dans les yeux non-traités (injection simulée ou sham). 5 ans après le traitement, l’amélioration bilatérale à partir du nadir a été maintenue, les yeux traités par LUMEVOQ® obtenant une amélioration moyenne par rapport au nadir de +22,0 lettres et les yeux sham montrant une amélioration moyenne de +19,5 lettres.
L’impact de ces résultats sur les patients est démontré par une amélioration des scores de qualité de vie (QoL) autodéclarés en Année 5 par rapport à la baseline. La qualité de vie globale moyenne a progressé de manière cliniquement significative par rapport à la baseline, portée par des améliorations des sous-scores pertinents correspondant à la santé mentale et à la capacité à mener des activités de manière autonome (par exemple, score composite, santé mentale, limites fonctionnelles, dépendance, activités faisant intervenir la vision de près et de loin, fonctionnement social).
« Les données à 5 ans de l’étude d’extension à long terme RESTORE illustrent le maintien de l’efficacité et de l’innocuité précédemment rapportées à la suite du traitement par une injection unique de LUMEVOQ, ce qui donne de l’espoir aux patients atteints de cette maladie cécitante« , a déclaré Patrick Yu-Wai-Man, MD, PhD, Moorfields Eye Hospital et Département de Neurosciences Cliniques, Université de Cambridge, Royaume-Uni.
« Les données recueillies jusqu’à présent, qui montrent l’efficacité soutenue de LUMEVOQ, combinée à un profil d’innocuité favorable, sont tout à fait conformes avec les convictions des experts cliniques selon lesquelles les effets de la thérapie génique ne s’estomperont pas après son administration« , a noté Magali TAIEL, MD, Directrice Médicale de GenSight Biologics. « Ayant une confiance renforcée dans le bénéfice que nous pouvons apporter aux patients, l’équipe de GenSight met toute son énergie afin de donner accès à notre thérapie aux patients de la façon la plus rapide et la plus sûre possible. »
RESTORE est une étude importante de suivi à long terme pour le traitement d’une maladie rare. 62 sujets ont accepté d’être inclus et suivis et 55 ont terminé l’étude. Tous les sujets atteints de NOHL causée par un gène mitochondrial ND4 muté ont été traités par une injection intravitréenne unique de LUMEVOQ® dans un œil et par une injection simulée (sham) dans l’autre.
Table 1. Amélioration de l’acuité visuelle (BCVA) par rapport au Nadir* dans l’étude de suivi à long terme de LUMEVOQ® (RESTORE)
| 2 ans post injection
(début de RESTORE) |
5 ans post injection4
(Fin de RESTORE) |
|||
| LogMAR
(Erreur Standard) |
Lettres ETDRS** | LogMAR (Erreur Standard) | Lettres ETDRS ** | |
| Yeux traités avec LUMEVOQ® | -0.38
(0.31) |
+18,8
|
-0.44
(0.46) |
+22,0
|
| Yeux Sham | -0.35
(0.29) |
+17,3
|
-0.39
(0.36) |
+19,5
|
Note : L’échantillon RESTORE est composé des participants aux études RESCUE et REVERSE qui ont accepté d’être suivis dans le cadre de l’étude de suivi à long terme. Les valeurs de l’année 5 étaient les mesures exprimées en LogMAR les plus proches de 1825 jours après le traitement enregistrées à 1 825 +/- 28 jours après le traitement. Les valeurs manquantes ont été imputées à l’aide de la méthode de la dernière observation reportée (LOCF).
*Nadir = acuité visuelle la plus basse enregistrée entre la baseline et l’année 5.
** Les mesures d’acuité visuelle ont été enregistrées en LogMAR. Le changement depuis le nadir en LogMAR a été converti en « équivalent lettres ETDRS » en multipliant le LogMAR par -50 (réf. J.T. Holladay, J Refrac Surgery, 1997 ;13, 388-391).
Les analyses des répondeurs à 5 ans indiquent qu’une proportion importante des patients suivis ont présenté une amélioration de l’acuité visuelle. 71,0% des sujets RESTORE ont ainsi obtenu une récupération cliniquement pertinente (Clinically Relevant Recovery ou CRR)5 par rapport au nadir 5 ans après le traitement, et 80,7% d’entre eux avaient une vision « on chart » (acuité visuelle ≤ 1,6 LogMAR, correspondant à la faculté de lire a minima 5 lettres ETDRS à 1m de distance) dans un ou les deux yeux.
Figure 1. Evolution de l’acuité visuelle chez les patients traités avec LUMEVOQ® (RESCUE/REVERSE/RESTORE) comparé aux patients non traités
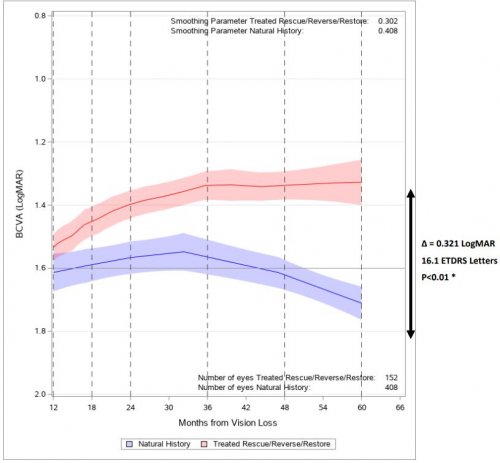
Note : Les courbes obtenues selon la méthode Locally Estimated Scatterplot Smoothing (LOESS) montrent l’évolution de l’acuité visuelle de 12 à 60 mois après le début de la perte de vision de tous les yeux (LUMEVOQ® et Sham) issus des études REVERSE / RESCUE / RESTORE, et de tous yeux d’une cohorte comparable de patients non traités par LUMEVOQ®. Les zones colorées représentent l’intervalle de confiance à 95% pour les valeurs de la BCVA. Les valeurs >60 mois ont été fixées à 60 mois. La courbe commence 12 mois après le début de la maladie lorsque 92,7% des yeux des études RESCUE et REVERSE ont reçu un traitement, soit avec LUMEVOQ®, soit avec une injection Sham. La cohorte non traitée était composée de 208 patients ND4-LHON qui ont été suivis dans le registre REALITY et issus de deux études d’histoire naturelle prospectives et huit rétrospectives.6
* p<0,01 pour le test de Kruskal-Wallis et les mesures répétées sur le patient.
Les résultats de sécurité 5 ans après l’injection sont cohérents avec les informations précédemment rapportées, qui concluaient que LUMEVOQ® est bien toléré : aucun événement indésirable grave n’a été enregistré parmi les yeux traités par LUMEVOQ®, et aucune sortie de l’étude n’est survenue en raison d’événements oculaires. Il n’y a pas eu d’événements indésirables graves systémiques ou de sorties liés au traitement ou à la procédure de l’étude.
L’examen de la demande d’Autorisation de Mise sur le Marché (AMM) européenne de LUMEVOQ® est en cours, et la décision du CHMP est attendue au troisième trimestre 2023 suite à une prolongation accordée par l’EMA pour les réponses de GenSight aux questions à 120 jours (D120). Le lancement commercial est prévu dans le prolongement de l’approbation d’ici la fin de l’année 2023.
Références and notes:
- Newman NJ, Yu-Wai-Man P, Carelli V, et al.,. Intravitreal Gene Therapy vs. Natural History in Patients With Leber Hereditary Optic Neuropathy Carrying the m.11778G>A ND4 Mutation: Systematic Review and Indirect Comparison. Neurol. (2021) 12:662838. doi: 10.3389/fneur.2021.662838.
- Biousse, V, Newman, N, Yu-Wai-Man P, et al. Long-Term Follow-Up After Unilateral Intravitreal Gene Therapy for Leber Hereditary Optic Neuropathy: The RESTORE Study, J Neuroophthalmol. (2021) 41: 309-315. doi: 10.1097/WNO.0000000000001367.
- Newman NJ, Yu-Wai-Man P, Carelli V, et al. Efficacy and safety of intravitreal gene therapy for Leber hereditary optic neuropathy treated within 6 months of disease onset. Ophthalmology (2021) 128:649–60. doi: 10.1016/j.ophtha.2020.12.012.
- Yu-Wai-Man P, Newman NJ, Carelli V, et al. Bilateral visual improvement with unilateral gene therapy injection for Leber hereditary optic neuropathy. Sci Transl Med. (2020) 12:eaaz7423. doi: 10.1126/scitranslmed.aaz7423.
- Clinically Relevant Recovery (CRR) corresponds to an improvement of at least 0.2 LogMAR (for on-chart eyes) or a movement from off-chart to on-chart (for off-chart eyes).
- Newman NJ, Yu-Wai-Man P, Carelli V, et al. Intravitreal gene therapy vs. natural history in patients with Leber hereditary optic neuropathy carrying the m.11778G>A ND4 mutation: systematic review and indirect comparison. Front Neurol. 2021;12:662838.
Contacts
-
Image7Communication et Relations PresseJulia Friedlander-Most / Romain Grière+33 (0)6 83 00 97 55 / +33 (0)7 86 53 17 29
-
LifeSci AdvisorsRelations InvestisseursGuillaume van Renterghem+41 (0)76 735 01 31
-
Orpheon FinanceInvestisseurs ParticuliersJames Palmer+33 7 60 92 77 74